Magnetismo dell'acciaio
1. MAGNETISMO E PROPRIETA’ MAGNETICHE
Il ferromagnetismo è il meccanismo attraverso il quale i materiali sono attratti dai magneti e formano magneti permanenti.

Per spiegare questo meccanismo dobbiamo partire dall’atomo di ferro (Fe) che ha un nucleo composto da 26 protoni e una trentina di neutroni intorno al quale orbitano 26 elettroni.
Questi 26 elettroni sono distribuiti attorno al nucleo in orbite particolari caratterizzate da livelli energetici distinti.
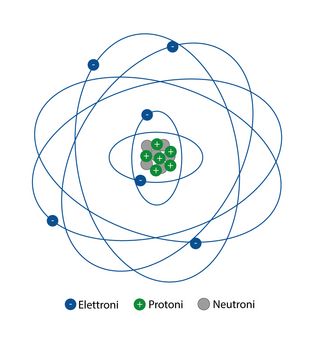
Consideriamo:
• 7 livelli energetici (1-2-3-4-5-6-7) (Il primo è il più vicino al nucleo)
• 4 tipi di orbitale (s-p-d-f)
Ogni orbitale può contenere al massimo 2 elettroni e la configurazione elettronica ci indica come essi si dispongono nei vari orbitali.
Con la regola della diagonale si può vedere l’ordine di riempimento dei vari livelli di energia:
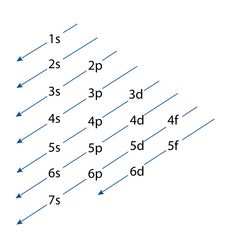
Ricordando che:
• Nell'orbitale s possono essere collocati al massimo 2 elettroni
• Nell'orbitale p possono essere collocati al massimo 6 elettroni
• Nell'orbitale d possono essere collocati al massimo 10 elettroni
• Nell'orbitale f possono essere collocati al massimo 14 elettroni
Possiamo scrivere la configurazione elettronica del ferro andando a posizionare i nostri 26 elettroni nei vari orbitali seguendo (più o meno…) la regola della diagonale:
1s2 2s2 2p6 3s2 3p6 4s2 3d6
Di regola l'orbitale è indicato con un quadrante in cui sono riportati con frecce il numero di elettroni presenti:
• 2 frecce = doppietto elettronico -> orbitale completo
• 1 freccia = elettrone disaccoppiato
• 0 frecce = assenza di elettroni
L'elettrone è considerato in continuo movimento attorno al nucleo, e siccome è una carica negativa genererà attorno alla sua orbita un campo magnetico.
Questo campo magnetico è generato da due movimenti:
• movimento dell'elettrone sulla sua orbita (momento orbitale)
• movimento di rotazione dell'elettrone su sé stesso (momento di spin), che è da considerarsi più importante.
Quando un orbitale è completo, i due elettroni che lo compongono sono di spin opposto, e quindi si annullano a vicenda.
Quando invece un orbitale è incompleto, contiene cioè un elettrone disaccoppiato, il suo momento di spin non sarà annullato dall'elettrone gemello, e l'elettrone presenterà un momento magnetico rappresentato dalla somma algebrica del suo momento di spin e di quello orbitale.
Torniamo alla configurazione elettronica del ferro: 1s2 2s2 2p6 3s2 3p6 4s2 3d6
L’orbitale d, che potrebbe contenere 10 elettroni, ne contiene 6, dunque ci sono 4 elettroni disaccoppiati che spiegano il comportamento ferromagnetico del ferro su scala microscopica.
RAPPRESENTAZIONE GRAFICA DELLA CONFIGURAZIONE ELETTRONICA DEL FERRO
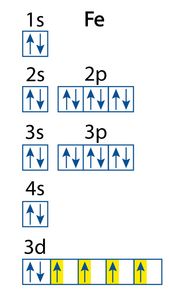
Per spiegare i fenomeni magnetici su scala macroscopica si parla di campo magnetico elementare che è da intendersi una regione delimitata della sostanza con momenti magnetici allineati uniformemente (cioè con spin allineati uniforme mente). Questi campi magnetici elementari, in assenza di un campo magnetico esterno, sono distribuiti casualmente col risultato di annullarsi a vicenda. Quando però agisce un campo esterno (es. un magnete), i momenti magnetici si orientano tutti nella stessa direzione acquistando quindi anch'essi la caratteristica di tutti i corpi magnetici e cioè la polarità.
ASSI DEI CRISTALLI
STATO NON MAGNETICO (campi elementari orientati casualmente)
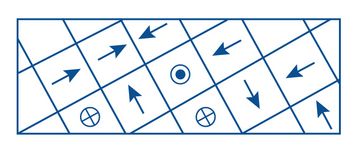
MAGNETIZZAZIONE (campi elementari orientati nello stesso senso)

2. CARATTERISTICHE MAGNETICHE DEGLI ACCIAI INOSSIDABILI
Esistono tre macro tipologie di acciai inossidabili che presentano strutture reticolari e comportamenti magnetici diversi:
• Ferritici (es. AISI 430) che hanno struttura Cubica a Corpo Centrato (CCC) e sono magnetici
• Austenitici (es. AISI 304 – AISI 316) che hanno struttura Cubica a Facce Centrate (CFC) e non sono magnetici
• Martensitici (es. AISI 420) che hanno struttura Cubica a Corpo Centrato (CCC) e sono magnetici
Il tipo più diffuso di acciaio inossidabile, il tipo 304, contiene ferro, cromo e nichel (ciascuno magnetico a sé stante) ma risulta non magnetico perché nella struttura a facce centrate (CFC) gli elettroni fanno fatica ad allineare la loro rotazione in una direzione sola.
Il tipo 304 può però diventare parzialmente magnetico dal momento che l’incrudimento che si determina in fase di stampaggio genera strutture pseudomartensitiche a corpo centrato (CCC) che sono magnetiche e lo stampo stesso può contaminare il pezzo fissandoci residui ferromagnetici. Tale effetto, se sgradito, si può limitare passando a materiale inossidabili più nobili tipo A4 e A4 low carbon.